作者:Alulul l时间:2016-06-28 10:52
从人工晶状体到角膜移植,为了拯救“心灵的窗户”,科学家和医生们可谓使尽了浑身解数。而在人造材料和器官捐献之外,干细胞现在也成了帮助人们恢复光明的新生力量。在3月9日的《自然》期刊上,就有两项新研究向世人展示了干细胞修复眼睛的新潜能。

自:shutterstock
治疗先天性白内障,晶状体也能“原地复活”
白内障患者眼睛里的晶状体变得浑浊,这会导致视力不断下降,它也是致盲的首要原因。一般来说,要想治疗白内障,就要去掉浑浊的晶状体,然后再植入人工晶体。不过,这种手术并不完美,它也受到并发症的限制,在发育尚不成熟的婴幼儿患者身上,这些问题尤其突出。
而现在,来自中山大学中山眼科中心与加州大学圣地亚哥分校的研究人员为先天性白内障患儿设计出了一种更加巧妙的治疗方案[1]。这一次,他们没有植入人工晶体,而是尽可能保全眼球中负责形成晶状体的干细胞,并让它们自行生长,产生新的晶状体。
研究者们首先在体外实验中验证了晶状体上皮干细胞(lens epithelial stem/progenitor cells, LECs)的修复潜力,接下来,他们在兔子和猕猴身上进行了新型手术方法的试验,又进行了小规模的临床试验。和传统的手术不同,这种手术方法缩小了切口,把切口挪到了不影响视轴区域的侧面,并尽可能地保留了患者自身的晶状体上皮干细胞。
12名年龄在2岁以下的先天性白内障小患者接受了这种新式手术,术后观察表明,所有小病人都在手术3个月后重新长出了清澈透明的晶状体,视力恢复情况也与接受常规手术的对照组相当。而且,这些依靠自身干细胞“自然生长”的新晶体发生视轴区浑浊等并发症的频率也比对照组少得多。
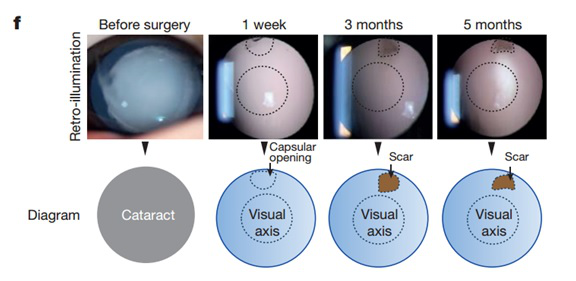
新的手术方法疤痕尺寸直径小于1.5毫米且不在视轴中央,术后患者晶状体均恢复透明,5个月内没有观察到任何异常的组织增生。图片来自:Lin et al. 2016
目前,这种技术还需要经过更多验证才能进行推广。考虑到眼部组织特性和组织再生能力的差异,想要把它用在成年人身上,也要克服不少困难。不过,这一结果确实让科学家们对干细胞与眼部组织修复有了新的认识,这也是人们第一次利用身体内源的干细胞完成了眼睛晶状体的修复。
培养皿里的“二次元眼睛”
在“原地复活”的晶状体之外,同期发表的另外一项研究显得更有几分科幻色彩。在这项研究中,来自日本的研究团队直接用干细胞在培养皿中“种”出了眼睛的雏形[2]。
在这里,研究者们使用的是近年来备受青睐的诱导多能干细胞(iPS)。在此之前,已经有不少研究尝试过把iPS细胞分化成各种各样的人体组织,不过这一次,研究者们可不满足于此——他们想要尝试的是用干细胞还原出整个眼球的发育过程。
为了实现这一设想,研究人员在iPS细胞生长的各个阶段使用了不同成分的培养介质,分步诱导iPS分化为不同种类的细胞。这些细胞聚集在一起,形成了一个个同心圆结构的细胞群。
在这个细胞群中,可以看到各种有序排列的眼球组织。通过检测,研究人员锁定了这些组织细胞的“身份”:位于中央1区的是神经外胚层细胞,略靠外的2区是神经视网膜细胞、神经脊以及类视网膜色素上皮细胞组,2区和3区之间零散分布着一些晶状体细胞团,3区是眼表上皮细胞,最外圈的4区则在将来可能会进一步分化为表皮角质形成细胞。这些区域分别对应着眼球上的多种重要组织,从晶状体、视网膜到视神经都可以找到对应,它就像是生长在培养皿中的“2D眼球”一样。
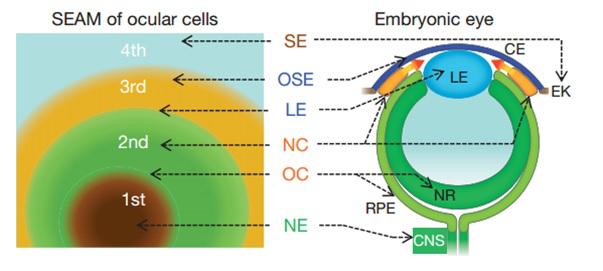
培养皿中的2D眼睛雏形中可以找到与眼球各部分对应的细胞。图片来自:Hayashi et al. 2016
有了这些培养皿中的“眼睛”,进行眼睛发育的研究就变得格外方便了。而且,这些人工培养的组织同样具有修复眼睛的潜力。从“培养皿眼睛”中分离出具有角膜上皮细胞特征的细胞继续培养,就能让它们成长为完整的角膜上皮。患有角膜干细胞缺陷的兔子在植入这些人工培养的角膜之后,也成功恢复了正常的角膜功能。
研究人员指出,虽然过去已有使用成体干细胞修复眼表组织的先例,但长期的治效并不理想,而培养皿中的“眼睛”或许能填补这一空白,与此同时,它也可以成为模拟眼球发育的模型,为今后的研究提供帮助。目前,他们正在着手启动首批人类临床试验。在将来,干细胞技术还将有望让更多人重获光明。
(编辑:不启轩)
文章题图:shutterstock 友情提供
参考资料:
1. Lin, Haotian, et al. "Lens regeneration using endogenous stem cells with gain of visual function." Nature 531.7594 (2016): 323-328.
2. Hayashi, Ryuhei, et al. "Co-ordinated ocular development from human iPS cells and recovery of corneal function." Nature 531.7594 (2016): 376-380.
(来源:科普中国kepuchina.org与果壳网guokr.com)
从人工晶状体到角膜移植,为了拯救“心灵的窗户”,科学家和医生们可谓使尽了浑身解数。而在人造材料和器官捐献之外,干细胞现在也成了帮助人们恢复光明的新生力量。在3月9日的《自然》期刊上,就有两项新研究向世人展示了干细胞修复眼睛的新潜能。

自:shutterstock
治疗先天性白内障,晶状体也能“原地复活”
白内障患者眼睛里的晶状体变得浑浊,这会导致视力不断下降,它也是致盲的首要原因。一般来说,要想治疗白内障,就要去掉浑浊的晶状体,然后再植入人工晶体。不过,这种手术并不完美,它也受到并发症的限制,在发育尚不成熟的婴幼儿患者身上,这些问题尤其突出。
而现在,来自中山大学中山眼科中心与加州大学圣地亚哥分校的研究人员为先天性白内障患儿设计出了一种更加巧妙的治疗方案[1]。这一次,他们没有植入人工晶体,而是尽可能保全眼球中负责形成晶状体的干细胞,并让它们自行生长,产生新的晶状体。
研究者们首先在体外实验中验证了晶状体上皮干细胞(lens epithelial stem/progenitor cells, LECs)的修复潜力,接下来,他们在兔子和猕猴身上进行了新型手术方法的试验,又进行了小规模的临床试验。和传统的手术不同,这种手术方法缩小了切口,把切口挪到了不影响视轴区域的侧面,并尽可能地保留了患者自身的晶状体上皮干细胞。
12名年龄在2岁以下的先天性白内障小患者接受了这种新式手术,术后观察表明,所有小病人都在手术3个月后重新长出了清澈透明的晶状体,视力恢复情况也与接受常规手术的对照组相当。而且,这些依靠自身干细胞“自然生长”的新晶体发生视轴区浑浊等并发症的频率也比对照组少得多。

新的手术方法疤痕尺寸直径小于1.5毫米且不在视轴中央,术后患者晶状体均恢复透明,5个月内没有观察到任何异常的组织增生。图片来自:Lin et al. 2016
目前,这种技术还需要经过更多验证才能进行推广。考虑到眼部组织特性和组织再生能力的差异,想要把它用在成年人身上,也要克服不少困难。不过,这一结果确实让科学家们对干细胞与眼部组织修复有了新的认识,这也是人们第一次利用身体内源的干细胞完成了眼睛晶状体的修复。
培养皿里的“二次元眼睛”
在“原地复活”的晶状体之外,同期发表的另外一项研究显得更有几分科幻色彩。在这项研究中,来自日本的研究团队直接用干细胞在培养皿中“种”出了眼睛的雏形[2]。
在这里,研究者们使用的是近年来备受青睐的诱导多能干细胞(iPS)。在此之前,已经有不少研究尝试过把iPS细胞分化成各种各样的人体组织,不过这一次,研究者们可不满足于此——他们想要尝试的是用干细胞还原出整个眼球的发育过程。
为了实现这一设想,研究人员在iPS细胞生长的各个阶段使用了不同成分的培养介质,分步诱导iPS分化为不同种类的细胞。这些细胞聚集在一起,形成了一个个同心圆结构的细胞群。
在这个细胞群中,可以看到各种有序排列的眼球组织。通过检测,研究人员锁定了这些组织细胞的“身份”:位于中央1区的是神经外胚层细胞,略靠外的2区是神经视网膜细胞、神经脊以及类视网膜色素上皮细胞组,2区和3区之间零散分布着一些晶状体细胞团,3区是眼表上皮细胞,最外圈的4区则在将来可能会进一步分化为表皮角质形成细胞。这些区域分别对应着眼球上的多种重要组织,从晶状体、视网膜到视神经都可以找到对应,它就像是生长在培养皿中的“2D眼球”一样。

培养皿中的2D眼睛雏形中可以找到与眼球各部分对应的细胞。图片来自:Hayashi et al. 2016
有了这些培养皿中的“眼睛”,进行眼睛发育的研究就变得格外方便了。而且,这些人工培养的组织同样具有修复眼睛的潜力。从“培养皿眼睛”中分离出具有角膜上皮细胞特征的细胞继续培养,就能让它们成长为完整的角膜上皮。患有角膜干细胞缺陷的兔子在植入这些人工培养的角膜之后,也成功恢复了正常的角膜功能。
研究人员指出,虽然过去已有使用成体干细胞修复眼表组织的先例,但长期的治效并不理想,而培养皿中的“眼睛”或许能填补这一空白,与此同时,它也可以成为模拟眼球发育的模型,为今后的研究提供帮助。目前,他们正在着手启动首批人类临床试验。在将来,干细胞技术还将有望让更多人重获光明。
(编辑:不启轩)
文章题图:shutterstock 友情提供
参考资料:
1. Lin, Haotian, et al. "Lens regeneration using endogenous stem cells with gain of visual function." Nature 531.7594 (2016): 323-328.
2. Hayashi, Ryuhei, et al. "Co-ordinated ocular development from human iPS cells and recovery of corneal function." Nature 531.7594 (2016): 376-380.
(来源:科普中国kepuchina.org与果壳网guokr.com)